化學示範實驗:自製焰色試驗棒演示焰色試驗(Homemade Flame Test Stick for Flame Test)〔I〕
國立玉里高級中學化學科黃有道老師 / 國立彰化師範大學化學系楊水平副教授責任編輯
前言
小朋友玩的仙女棒,慶典晚會的煙火,各種火焰顏色應有盡有,這些焰色是怎麼產生的呢?本示範實驗採用兩種焰色試驗,其一為使用自製的焰色試驗棒和本生燈來 試驗鹽類固體,其二為使用卡式瓦斯噴燈和噴霧瓶來試驗鹽類水溶液。自製的焰色試驗棒取自於報廢的開飲機之加熱片並製作而得的,而且焰色試驗的效果很好,值 得教師參考。
示範步驟
A. 示範前準備
A1. 自製焰色試驗棒
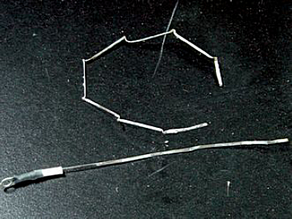
1. 從報廢的開飲機、電熱水瓶或電鍋取出加熱片,如圖一所示。
2. 用尖嘴鉗拆解加熱片,即可見到加熱片中的鎳鉻絲,這種鎳鉻絲的寬度約1 mm,如圖二所示。
3.
拆下加熱片的鎳鉻絲,並剪下連接電源端的直條鎳鉻絲,如圖三所示。
4. 用尖嘴鉗剪斷加熱片的鎳鉻絲成為每段長度20-25
cm,在末端處捲成小圓圈,另一端用銅線綁住衛生筷,便完成一支自製焰色試驗棒,如圖四所示。
A2. 準備金屬鹽類及配製水溶液
1. 準備少量的金屬鹽類:鋰、鈉、鉀、鈣、鍶、鋇、銅、鐵、鉛、鋅等實驗室常見的氯化物、硝酸鹽或硫酸鹽均可。2. 配製50 mL的金屬鹽類水溶液(濃度約1 M,濃度是可變的):鋰、鈉、鉀、鈣、鍶、鋇、銅、鐵、鉛、鋅等實驗室常見的氯化物、硝酸鹽或硫酸鹽均可。這些水溶液可裝在小型噴霧罐,並加入少量的酒精或甲醇,如圖五的左圖所示。
3. 配製50 mL的1 M鹽酸水溶液。
4. 準備一支卡式瓦斯噴燈,如圖五的右圖所示。
B. 正式示範
B1. 使用自製焰色試驗棒1. 點燃本生燈,調節瓦斯流量及空氣流量的旋轉鈕,以獲得理想的無光焰(淡藍色火焰),如圖六的左圖所示。自製焰色試驗棒的鎳鉻絲先沾稀鹽酸進行酸洗,再放置於本生燈的火焰上燒至火紅,如圖六的右圖所示。
2.
鎳鉻絲燒至火紅後,沾蒸餾水再次燒至火紅,然後沾一種金屬鹽類固體,放置於本生燈的火焰上燒,觀察火焰的顏色,如圖七所示。
3. 重複步驟2,使用不同金屬鹽類進行焰色試驗。
B2. 使用卡式瓦斯噴燈1. 打開卡式瓦斯噴燈,調整適當的火力,讓學生觀察無光焰(藍色火焰),如圖八所示。
2.
使用裝蒸餾水的噴霧罐斜向地噴射瓦斯噴燈的火焰,噴霧方向與噴火方向應盡可能同向,觀察水霧與火焰接觸時火焰的顏色。
3. 使用裝有硫酸銅(或氯化銅)水溶液的噴霧罐重複步驟2.,觀察火焰的顏色,如圖九所示。
4. 使用裝有氯化鈉水溶液的噴霧罐重複步驟2.,觀察火焰的顏色,如圖十所示。
5. 依次使用各種不同金屬鹽類水溶液進行上述試驗,觀察火焰的顏色。
藥品與器材1. 報廢的飲水機、電熱水瓶或電鍋(含加熱片的鎳鉻絲) 1台
2. 尖嘴鉗 1支
3. 銅線(細) 10-20 cm
4. 衛生筷 1支
5. 卡式瓦斯噴燈 1個
6. 小型噴霧罐(100 mL) 1個
7. 金屬鹽類常見的氯化物、硝酸鹽或硫酸鹽 少量
8. 金屬鹽類水溶液(濃度約1 M):常見的氯化物、硝酸鹽或硫酸鹽 各50 mL
9. 1 M鹽酸 100 mL
10. 蒸餾水 少許
11. 本生燈 1個
12. 酒精或甲醇(可選擇) 少量
原理和概念
● 本生燈或瓦斯噴燈的火焰為淡藍色,光度極低,此火焰稱為無光焰。
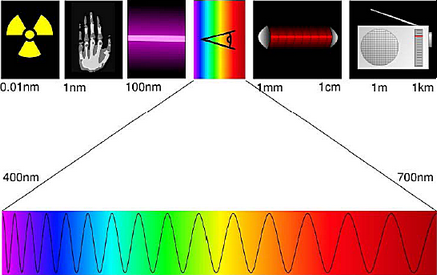
● 光是一種電磁波,一般人的眼睛可以感受的電磁波波長在400(紫色)到700(紅色)奈米(nm)之間,如圖十一所示。
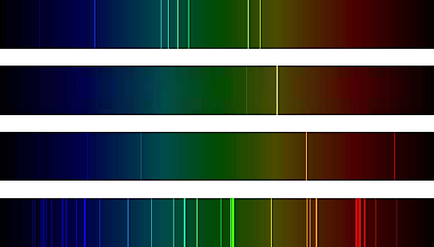
● 當一個元素被激發(加熱)時,其電子會躍遷至能量較高的軌域上。當它返回低能量的軌域時,高低軌域的能量差會以電磁波的形式輻射出來,出現在某些特定的波
長上,稱為發射光譜。每種元素都有其個別的光譜,這些譜線就好比人類的指紋一般,科學家可據以鑑定元素,如圖十二所示。
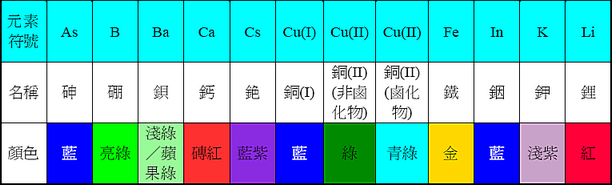
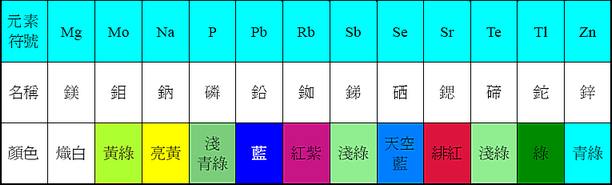
● 一些常見的金屬與其相對應的火焰顏色,如表一所示:
表一 一些常見的金屬與其相對應的火焰顏色
● 工業用途上的焰色試驗:在部分工業上會使用焰色試驗,這是因為聚合物、金屬類會發出許多獨特的燃燒方式,所以在鑑定聚合物及金屬化合物上是特別有用的。● 焰色試驗的限制:大部分離子在低濃度時無法做此試驗。從一個樣品到另一個樣品亮度會產生變化。例如:鈉所釋放出來的黃色光比鋰所釋放出的紅色光還要亮。由 於雜質或汙染物會影響試驗結果,尤其是大部分的化合物中都有鈉的存在而產生鈉的焰色,因此有時會使用一種藍色玻璃來過濾鈉的黃色焰色。由於若干金屬會產生 相同的焰色,此試驗無法完全區分所有元素,且有些化合物在燃燒時並不會改變其顏色。
教學提示
● 教師準備藥品與器材:30分鐘。課堂時間:5-10分鐘。本實驗教師可在教室或實驗室示範,也可以讓學生在實驗室操作。若由學生實驗操作,則操作時間為15-20分鐘。
● 本示範實驗可以融入原子發射光譜、電磁波和金屬元素的性質於課堂教學中。
● 使用自製焰色試驗棒時,用溼潤的鎳鉻絲可以容易沾取金屬鹽類,方便進行焰色試驗。
● 示範時,瓦斯噴燈的噴火方向務必側對學生,不可面對學生,以策安全。噴霧方向與噴火方向應盡可能同向,而且盡量勿讓水霧落在噴燈金屬管上。
● 為加強焰色試驗的效果,可在金屬鹽類水溶液中加入一些酒精或甲醇,但不宜加入太多以免影響焰色。
● 可使用酒精燈代替本生燈,但其溫度較低效果較差。環境光害愈少(愈昏暗),焰色觀察愈容易。可使用參考資料第3.項「簡易直視型分光器」,讓學生觀察焰色。
問題
1. 日常生活中,哪些地方或場所可見到彩色的火焰?這些彩色的火焰是如何產生的?
2. 使用鎳鉻絲與噴霧示範焰色試驗各有甚麼優缺點?
3. 在化學分析上,為何常用焰色試驗來鑑定鹼金屬元素?
安全
● 請戴護目鏡和著實驗衣。注意用火安全,尤其是學生操作本生燈時。
● 示範這個實驗實行適當的風險評估是老師的責任。
資料來源
1. Flame test, http://en.wikipedia.org/wiki/Flame_test.
2. Flame tests, http://chemistry.about.com/od/analyticalchemistry/a/flametest.htm.
3. Flame Coloration by Element, http://webmineral.com/help/FlameTest.shtml.
4. 燄色試驗(Flame Test),http://highscope.ch.ntu.edu.tw/wordpress/?p=3522。
5. 焰色試驗法(flame test),http://highscope.ch.ntu.edu.tw/wordpress/?p=3504。
6. 察「焰」觀「色」-以自製分光儀檢視焰色實驗,http://science.ntsec.edu.tw/files/15-1004-11059,c2308-1.php。
7. 簡易直視型分光器的製作,http://a-chien.blogspot.com/2010/01/blog-post_3530.html。
以上文章引用自:http://highscope.ch.ntu.edu.tw/wordpress









沒有留言:
張貼留言